Modèle quantique de l’atome
DownloadTélécharger
Actions
Vote :
ScreenshotAperçu
Informations
Catégorie :Category: mViewer GX Creator Lua TI-Nspire
Auteur Author: arnaudtoni83
Type : Classeur 3.6
Page(s) : 4
Taille Size: 178.42 Ko KB
Mis en ligne Uploaded: 26/10/2020 - 09:23:36
Uploadeur Uploader: arnaudtoni83 (Profil)
Téléchargements Downloads: 19
Visibilité Visibility: Archive publique
Shortlink : https://tipla.net/a2650276
Type : Classeur 3.6
Page(s) : 4
Taille Size: 178.42 Ko KB
Mis en ligne Uploaded: 26/10/2020 - 09:23:36
Uploadeur Uploader: arnaudtoni83 (Profil)
Téléchargements Downloads: 19
Visibilité Visibility: Archive publique
Shortlink : https://tipla.net/a2650276
Description
Modèle quantique de l’atome
Nombres quantiques n, ℓ et mℓ
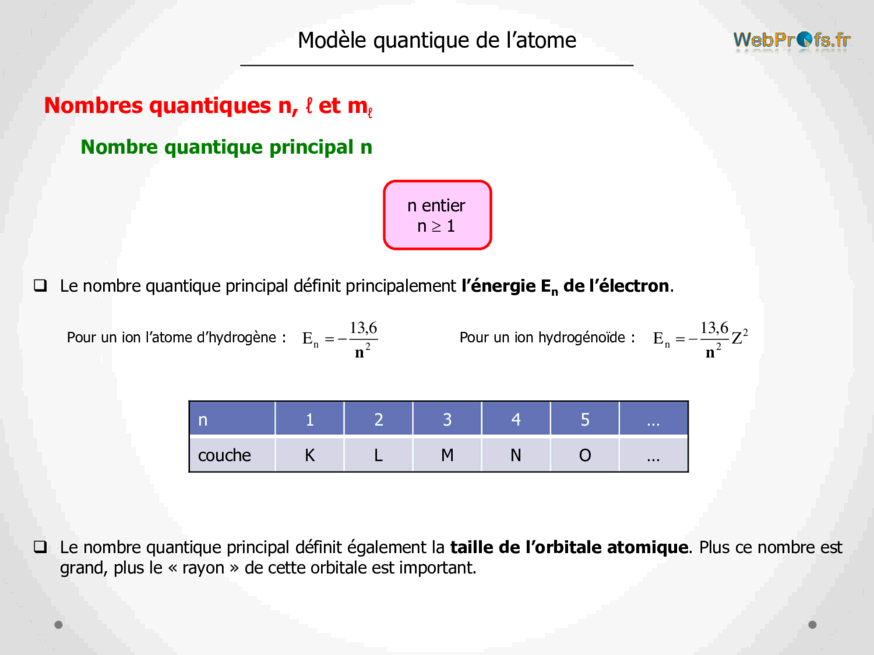
Nombre quantique principal n
n entier
n1
Le nombre quantique principal définit principalement l’énergie En de l’électron.
13,6 13,6 2
Pour un ion l’atome d’hydrogène : En Pour un ion hydrogénoïde : En Z
n2 n2
n 1 2 3 4 5 …
couche K L M N O …
Le nombre quantique principal définit également la taille de l’orbitale atomique. Plus ce nombre est
grand, plus le « rayon » de cette orbitale est important.
Modèle quantique de l’atome
Nombres quantiques n, ℓ et mℓ
Nombre quantique secondaire ou azimutal ℓ
ℓ entier
0ℓn-1
Le nombre quantique secondaire définit la sous-couche énergétique En,ℓ de l’électron.
ℓ 0 1 2 3 4 …
sous-couche s p d f g …
Le nombre quantique secondaire définit également la forme de l’orbitale atomique.
Modèle quantique de l’atome
Nombres quantiques n, ℓ et mℓ
Nombre quantique tertiaire ou magnétique mℓ
mℓ entier
-ℓ mℓ ℓ
Le nombre quantique magnétique n’intervient pas dans l’énergie électronique.
mℓ = 0 Energie
ℓ=0
n=2
mℓ =-1
Dégénérescence mℓ = 0
ℓ=1 mℓ = 0 E2,1
des niveaux d’énergie
mℓ =-1 mℓ = +1
mℓ = +1
Le nombre quantique magnétique précise l’orientation de l’orbitale atomique.
Modèle quantique de l’atome
Notation des orbitales atomiques
Chaque orbitale est nommée en fonction des 3 nombres quantiques qui la caractérisent. Elle porte dans
l’ordre d’écriture :
• La valeur du nombre quantique principal n
• La lettre associée au nombre quantique secondaire ℓ
• La valeur du nombre quantique magnétique mℓ (en indice)
Exemple :
• L’orbitale notée 4d-1 est caractérisée par le triplet (n = 4 ; ℓ = 2 ; mℓ = -1)
Nombres quantiques n, ℓ et mℓ
Nombre quantique principal n
n entier
n1
Le nombre quantique principal définit principalement l’énergie En de l’électron.
13,6 13,6 2
Pour un ion l’atome d’hydrogène : En Pour un ion hydrogénoïde : En Z
n2 n2
n 1 2 3 4 5 …
couche K L M N O …
Le nombre quantique principal définit également la taille de l’orbitale atomique. Plus ce nombre est
grand, plus le « rayon » de cette orbitale est important.
Modèle quantique de l’atome
Nombres quantiques n, ℓ et mℓ
Nombre quantique secondaire ou azimutal ℓ
ℓ entier
0ℓn-1
Le nombre quantique secondaire définit la sous-couche énergétique En,ℓ de l’électron.
ℓ 0 1 2 3 4 …
sous-couche s p d f g …
Le nombre quantique secondaire définit également la forme de l’orbitale atomique.
Modèle quantique de l’atome
Nombres quantiques n, ℓ et mℓ
Nombre quantique tertiaire ou magnétique mℓ
mℓ entier
-ℓ mℓ ℓ
Le nombre quantique magnétique n’intervient pas dans l’énergie électronique.
mℓ = 0 Energie
ℓ=0
n=2
mℓ =-1
Dégénérescence mℓ = 0
ℓ=1 mℓ = 0 E2,1
des niveaux d’énergie
mℓ =-1 mℓ = +1
mℓ = +1
Le nombre quantique magnétique précise l’orientation de l’orbitale atomique.
Modèle quantique de l’atome
Notation des orbitales atomiques
Chaque orbitale est nommée en fonction des 3 nombres quantiques qui la caractérisent. Elle porte dans
l’ordre d’écriture :
• La valeur du nombre quantique principal n
• La lettre associée au nombre quantique secondaire ℓ
• La valeur du nombre quantique magnétique mℓ (en indice)
Exemple :
• L’orbitale notée 4d-1 est caractérisée par le triplet (n = 4 ; ℓ = 2 ; mℓ = -1)












