Systeme à l'equilibre thermodynamique
DownloadTélécharger
Actions
Vote :
ScreenshotAperçu
Informations
Catégorie :Category: mViewer GX Creator Lua TI-Nspire
Auteur Author: omar1998
Type : Classeur 3.6
Page(s) : 13
Taille Size: 1.20 Mo MB
Mis en ligne Uploaded: 12/03/2019 - 17:48:21
Uploadeur Uploader: omar1998 (Profil)
Téléchargements Downloads: 45
Visibilité Visibility: Archive publique
Shortlink : https://tipla.net/a1971409
Type : Classeur 3.6
Page(s) : 13
Taille Size: 1.20 Mo MB
Mis en ligne Uploaded: 12/03/2019 - 17:48:21
Uploadeur Uploader: omar1998 (Profil)
Téléchargements Downloads: 45
Visibilité Visibility: Archive publique
Shortlink : https://tipla.net/a1971409
Description
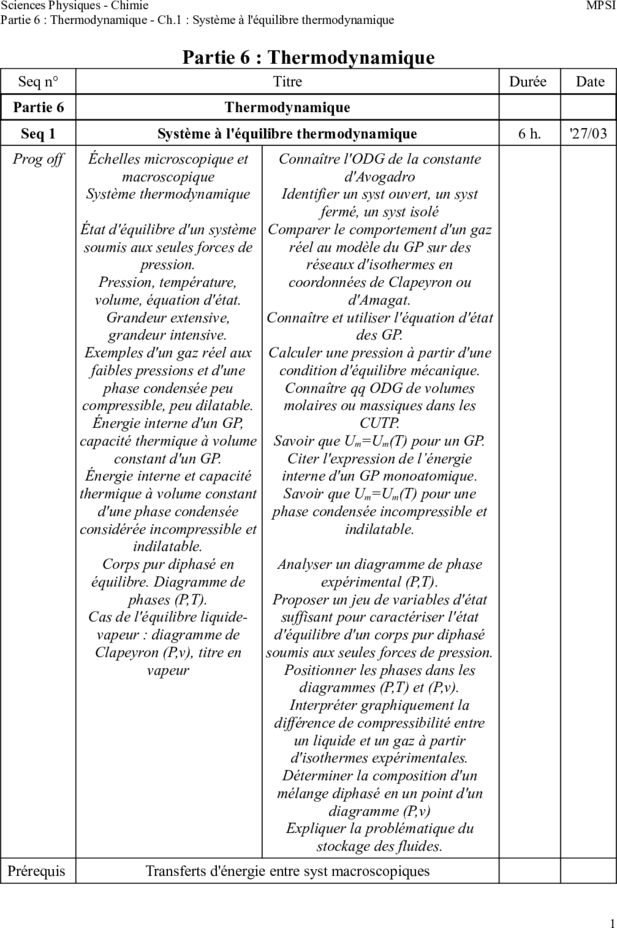
Sciences Physiques - Chimie MPSI
Partie 6 : Thermodynamique - Ch.1 : Système à l'équilibre thermodynamique
Partie 6 : Thermodynamique
Seq n° Titre Durée Date
Partie 6 Thermodynamique
Seq 1 Système à l'équilibre thermodynamique 6 h. '27/03
Prog off Échelles microscopique et Connaître l'ODG de la constante
macroscopique d'Avogadro
Système thermodynamique Identifier un syst ouvert, un syst
fermé, un syst isolé
État d'équilibre d'un système Comparer le comportement d'un gaz
soumis aux seules forces de réel au modèle du GP sur des
pression. réseaux d'isothermes en
Pression, température, coordonnées de Clapeyron ou
volume, équation d'état. d'Amagat.
Grandeur extensive, Connaître et utiliser l'équation d'état
grandeur intensive. des GP.
Exemples d'un gaz réel aux Calculer une pression à partir d'une
faibles pressions et d'une condition d'équilibre mécanique.
phase condensée peu Connaître qq ODG de volumes
compressible, peu dilatable. molaires ou massiques dans les
Énergie interne d'un GP, CUTP.
capacité thermique à volume Savoir que Um=Um(T) pour un GP.
constant d'un GP. Citer l'expression de l’énergie
Énergie interne et capacité interne d'un GP monoatomique.
thermique à volume constant Savoir que Um=Um(T) pour une
d'une phase condensée phase condensée incompressible et
considérée incompressible et indilatable.
indilatable.
Corps pur diphasé en Analyser un diagramme de phase
équilibre. Diagramme de expérimental (P,T).
phases (P,T). Proposer un jeu de variables d'état
Cas de l'équilibre liquide- suffisant pour caractériser l'état
vapeur : diagramme de d'équilibre d'un corps pur diphasé
Clapeyron (P,v), titre en soumis aux seules forces de pression.
vapeur Positionner les phases dans les
diagrammes (P,T) et (P,v).
Interpréter graphiquement la
différence de compressibilité entre
un liquide et un gaz à partir
d'isothermes expérimentales.
Déterminer la composition d'un
mélange diphasé en un point d'un
diagramme (P,v)
Expliquer la problématique du
stockage des fluides.
Prérequis Transferts d'énergie entre syst macroscopiques
1
Sciences Physiques - Chimie MPSI
Partie 6 : Thermodynamique - Ch.1 : Système à l'équilibre thermodynamique
Seq n° Titre Durée Date
Ouverture Énergie interne introduite en TaleS pour une phase condensée →
énergie interne, modification par W et Q → 1er principe
Diffusion thermique → irréversibilité
Ch.1 Système à l'équilibre thermodynamique 4h
I – Description micro et macro de la matière
II – Système thermodynamique
III – Équilibre thermodynamique
IV – Équation d'état
V – Corps pur diphasé en équilibre
VI – Équilibre liquide-gaz
VII – Énergie interne et CV
TP Non
TD Exercices 2h
DM
DS DS 7
Étude de la matière à l'échelle macroscopique → objectif : applications « motivantes ». Les
capacités doivent être introduites en s'appuyant dès que possible sur des dispositifs expérimentaux
pour permettre une acquisition progressive et authentique. Étude du corps pur, subissant des transfo
finies.
Pour les bilans finis d'énergie, les expressions des fonctions d'état U m(T,Vm) et Hm(T,P) seront
données si le système n'est pas « GP » ou « phase condensée incompressible et indilatable ».
Pour les bilans finis d'entropie, l'expression de la fonction d'état S sera donnée.
→ Application des principes de la thermodynamique aux machines thermiques avec écoulement
stationnaire → objectif : avoir compris pourquoi l'enthalpie intervient.
Rq : Orienter l'enseignement de la thermodynamique vers des applications industrielles réelles
motivantes grâce à l'utilisation de diagrammes.
Notation :
• Pour une grandeur extensive (additive) : A (ex : n, m, V)
• grandeur massique associée : a
• grandeur molaire associée : Am
• Compétences à développer :
◦ Rigueur des raisonnements : définition du système, lois utilisées, …
◦ Faire le lien entre un système réel et sa modélisation.
◦ Comprendre qu'il peut exister des modèles de complexité croissante pour rendre compte
des observations expérimentales.
◦ Utiliser des tableaux de données ou des représentations graphiques complexes.
• Compétences expérimentales :
◦ Mettre en œuvre un capteur, en distinguant son caractère différentiel ou absolu (pression,
température, …)
◦ Mettre en œuvre un capteur de température : thermomètre, thermistance ou capteur IR.
◦ Mettre en œuvre une technique de calorimétrie → effectuer des bilans d'énergie
2
Sciences Physiques - Chimie MPSI
Partie 6 : Thermodynamique - Ch.1 : Système à l'équilibre thermodynamique
Ch.1 Système à l'équilibre thermodynamique
La thermodynamique est une théorie qui va permettre l'étude de la matière à l'échelle
macroscopique en partant de considérations microscopiques. En résumé, on fait la moyenne sur les
23
N A=6,02 .10 particules qui composent 1 mol de tout corps et on en déduit le comportement de
ce corps à notre échelle.
Par exemple, il existe un lien entre agitation thermique des particules d'un gaz et température
de ce gaz. La température du gaz peut être vue comme la moyenne des énergies cinétiques des
3
particules qui composent ce gaz, sous la forme : k T =< E c > (avec kB : constante de Boltzman)
2 B
• Notations :
Les grandeurs extensives (additives) seront notées : A (ex : V, E(énergie), U(énergie interne …)
→ Grandeur massique associée : a
→ Grandeur molaire associée : Am
I. Description microscopique et macroscopique de la matière
I.1. Phases solide, liquide et gaz (ou vapeur)
On a déjà vu la distinction entre ces 3 phases (voir chimie – P4-ch.1).
Rappelons simplement que :
• Les phases solide et liquide ont des masses volumiques du même ODG (à connaître),
environ 1000 fois supérieur à l'ODG de la masse volumique d'un gaz. Ces 2 phases sont
appelées phases condensées.
Typiquement :
Fer Eau Air
(dans les CNTP)
Masse volumique ρ fer=7800 kg.m
−3
ρeau=1000 kg.m
−3
ρair≃1 kg.m
−3
Volume massique v mfer =1,3 .10−4 m3 . kg −1 v meau =10−3 m3 . kg −1 v mair ≃1 m3 . kg −1
1
vm= ρ
Le volume des phases condensées dépend peu de la température (phase indilatable) et
quasiment pas de la pression (phase incompressible).
• Les phases liquide et gaz peuvent s'écouler. Ces 2 phases sont appelées phases fluides.
I.2. Trois échelles de description : mic...
Partie 6 : Thermodynamique - Ch.1 : Système à l'équilibre thermodynamique
Partie 6 : Thermodynamique
Seq n° Titre Durée Date
Partie 6 Thermodynamique
Seq 1 Système à l'équilibre thermodynamique 6 h. '27/03
Prog off Échelles microscopique et Connaître l'ODG de la constante
macroscopique d'Avogadro
Système thermodynamique Identifier un syst ouvert, un syst
fermé, un syst isolé
État d'équilibre d'un système Comparer le comportement d'un gaz
soumis aux seules forces de réel au modèle du GP sur des
pression. réseaux d'isothermes en
Pression, température, coordonnées de Clapeyron ou
volume, équation d'état. d'Amagat.
Grandeur extensive, Connaître et utiliser l'équation d'état
grandeur intensive. des GP.
Exemples d'un gaz réel aux Calculer une pression à partir d'une
faibles pressions et d'une condition d'équilibre mécanique.
phase condensée peu Connaître qq ODG de volumes
compressible, peu dilatable. molaires ou massiques dans les
Énergie interne d'un GP, CUTP.
capacité thermique à volume Savoir que Um=Um(T) pour un GP.
constant d'un GP. Citer l'expression de l’énergie
Énergie interne et capacité interne d'un GP monoatomique.
thermique à volume constant Savoir que Um=Um(T) pour une
d'une phase condensée phase condensée incompressible et
considérée incompressible et indilatable.
indilatable.
Corps pur diphasé en Analyser un diagramme de phase
équilibre. Diagramme de expérimental (P,T).
phases (P,T). Proposer un jeu de variables d'état
Cas de l'équilibre liquide- suffisant pour caractériser l'état
vapeur : diagramme de d'équilibre d'un corps pur diphasé
Clapeyron (P,v), titre en soumis aux seules forces de pression.
vapeur Positionner les phases dans les
diagrammes (P,T) et (P,v).
Interpréter graphiquement la
différence de compressibilité entre
un liquide et un gaz à partir
d'isothermes expérimentales.
Déterminer la composition d'un
mélange diphasé en un point d'un
diagramme (P,v)
Expliquer la problématique du
stockage des fluides.
Prérequis Transferts d'énergie entre syst macroscopiques
1
Sciences Physiques - Chimie MPSI
Partie 6 : Thermodynamique - Ch.1 : Système à l'équilibre thermodynamique
Seq n° Titre Durée Date
Ouverture Énergie interne introduite en TaleS pour une phase condensée →
énergie interne, modification par W et Q → 1er principe
Diffusion thermique → irréversibilité
Ch.1 Système à l'équilibre thermodynamique 4h
I – Description micro et macro de la matière
II – Système thermodynamique
III – Équilibre thermodynamique
IV – Équation d'état
V – Corps pur diphasé en équilibre
VI – Équilibre liquide-gaz
VII – Énergie interne et CV
TP Non
TD Exercices 2h
DM
DS DS 7
Étude de la matière à l'échelle macroscopique → objectif : applications « motivantes ». Les
capacités doivent être introduites en s'appuyant dès que possible sur des dispositifs expérimentaux
pour permettre une acquisition progressive et authentique. Étude du corps pur, subissant des transfo
finies.
Pour les bilans finis d'énergie, les expressions des fonctions d'état U m(T,Vm) et Hm(T,P) seront
données si le système n'est pas « GP » ou « phase condensée incompressible et indilatable ».
Pour les bilans finis d'entropie, l'expression de la fonction d'état S sera donnée.
→ Application des principes de la thermodynamique aux machines thermiques avec écoulement
stationnaire → objectif : avoir compris pourquoi l'enthalpie intervient.
Rq : Orienter l'enseignement de la thermodynamique vers des applications industrielles réelles
motivantes grâce à l'utilisation de diagrammes.
Notation :
• Pour une grandeur extensive (additive) : A (ex : n, m, V)
• grandeur massique associée : a
• grandeur molaire associée : Am
• Compétences à développer :
◦ Rigueur des raisonnements : définition du système, lois utilisées, …
◦ Faire le lien entre un système réel et sa modélisation.
◦ Comprendre qu'il peut exister des modèles de complexité croissante pour rendre compte
des observations expérimentales.
◦ Utiliser des tableaux de données ou des représentations graphiques complexes.
• Compétences expérimentales :
◦ Mettre en œuvre un capteur, en distinguant son caractère différentiel ou absolu (pression,
température, …)
◦ Mettre en œuvre un capteur de température : thermomètre, thermistance ou capteur IR.
◦ Mettre en œuvre une technique de calorimétrie → effectuer des bilans d'énergie
2
Sciences Physiques - Chimie MPSI
Partie 6 : Thermodynamique - Ch.1 : Système à l'équilibre thermodynamique
Ch.1 Système à l'équilibre thermodynamique
La thermodynamique est une théorie qui va permettre l'étude de la matière à l'échelle
macroscopique en partant de considérations microscopiques. En résumé, on fait la moyenne sur les
23
N A=6,02 .10 particules qui composent 1 mol de tout corps et on en déduit le comportement de
ce corps à notre échelle.
Par exemple, il existe un lien entre agitation thermique des particules d'un gaz et température
de ce gaz. La température du gaz peut être vue comme la moyenne des énergies cinétiques des
3
particules qui composent ce gaz, sous la forme : k T =< E c > (avec kB : constante de Boltzman)
2 B
• Notations :
Les grandeurs extensives (additives) seront notées : A (ex : V, E(énergie), U(énergie interne …)
→ Grandeur massique associée : a
→ Grandeur molaire associée : Am
I. Description microscopique et macroscopique de la matière
I.1. Phases solide, liquide et gaz (ou vapeur)
On a déjà vu la distinction entre ces 3 phases (voir chimie – P4-ch.1).
Rappelons simplement que :
• Les phases solide et liquide ont des masses volumiques du même ODG (à connaître),
environ 1000 fois supérieur à l'ODG de la masse volumique d'un gaz. Ces 2 phases sont
appelées phases condensées.
Typiquement :
Fer Eau Air
(dans les CNTP)
Masse volumique ρ fer=7800 kg.m
−3
ρeau=1000 kg.m
−3
ρair≃1 kg.m
−3
Volume massique v mfer =1,3 .10−4 m3 . kg −1 v meau =10−3 m3 . kg −1 v mair ≃1 m3 . kg −1
1
vm= ρ
Le volume des phases condensées dépend peu de la température (phase indilatable) et
quasiment pas de la pression (phase incompressible).
• Les phases liquide et gaz peuvent s'écouler. Ces 2 phases sont appelées phases fluides.
I.2. Trois échelles de description : mic...












